近期,我校565net必赢客户端饶义剑教授团队系统地阐述了四氢异喹啉生物碱(THIAs)天然合成途径解析及微生物异源合成方面的研究进展,以“Elucidation and biosynthesis of tetrahydroisoquinoline alkaloids: Recent advances and prospects”为题正式发表于“Biotechnology Advances”(IF =/info/1021/ /12.1)(https://doi.org/10.1016/j.biotechadv.2025.108524)
THIAs是一类重要的植物次生代谢产物,具有广泛的药理活性,如镇痛、抗菌、抗癌等。然而,传统的植物提取方法效率低,难以满足市场需求。随着合成生物学和代谢工程的发展,利用微生物异源合成THIAs成为了一种极具潜力的替代方案。
近年来,随着基因组学、转录组学和代谢组学技术的进步,研究人员解析了多个THIAs的天然合成途径,特别是秋水仙碱、加兰他敏和原吐根碱(图1),为此类化合物的微生物异源合成提供了坚实的基础。通过结合蛋白质工程、辅因子工程和全局优化工程等手段,成功在大肠杆菌和酿酒酵母中实现了多种THIAs的高效合成,如吗啡、诺司卡品和血根碱等。通过构建人工多酶级联反应,简化了天然产物的合成步骤,有效地提高了终产物产量(图2)。此外,化学酶级联反应也为THIAs的合成提供了新的思路,结合化学合成和酶催化的优势,实现了复杂分子的高效合成(图3)。尽管目前仍面临THIAs在微生物异源合成产量低等挑战,但通过新酶挖掘、辅因子工程、模块化调控和设计人工多酶级联反应等策略,未来有望实现THIAs的工业化生产。这项研究为THIAs的高效生物合成提供了新的思路,预示着未来通过微生物工厂大规模生产这些高价值化合物的可能性。
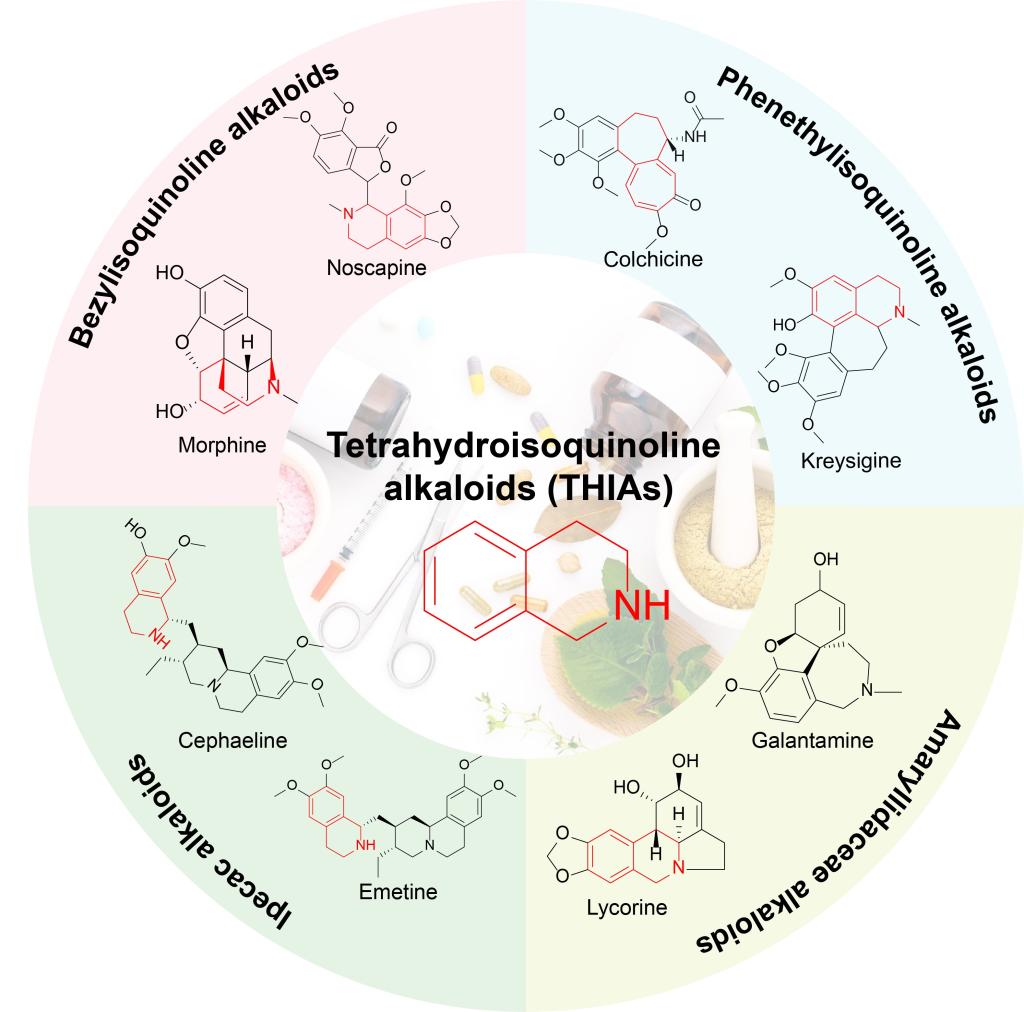
图1 基于前体骨架结构的THIAs分类
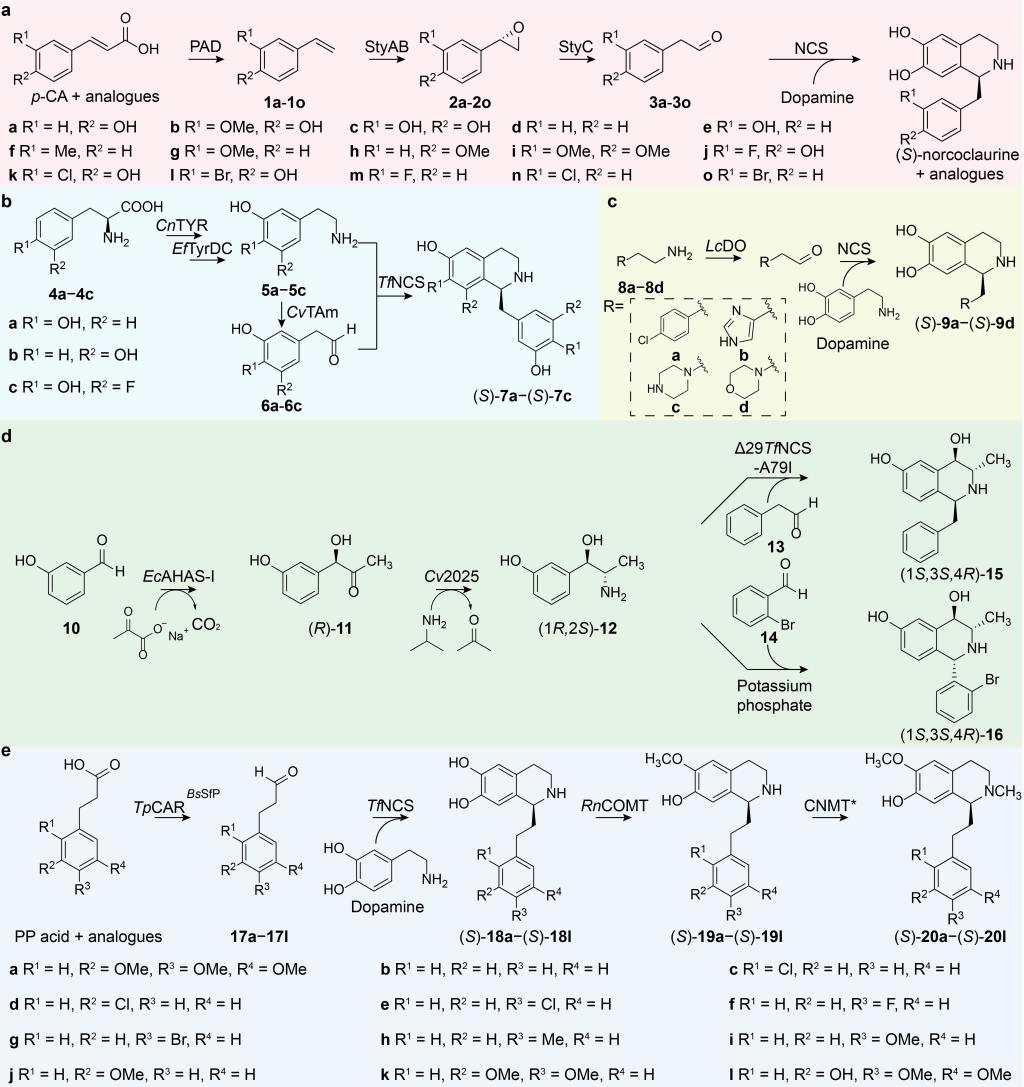
图2 合成THIAs的多酶级联反应
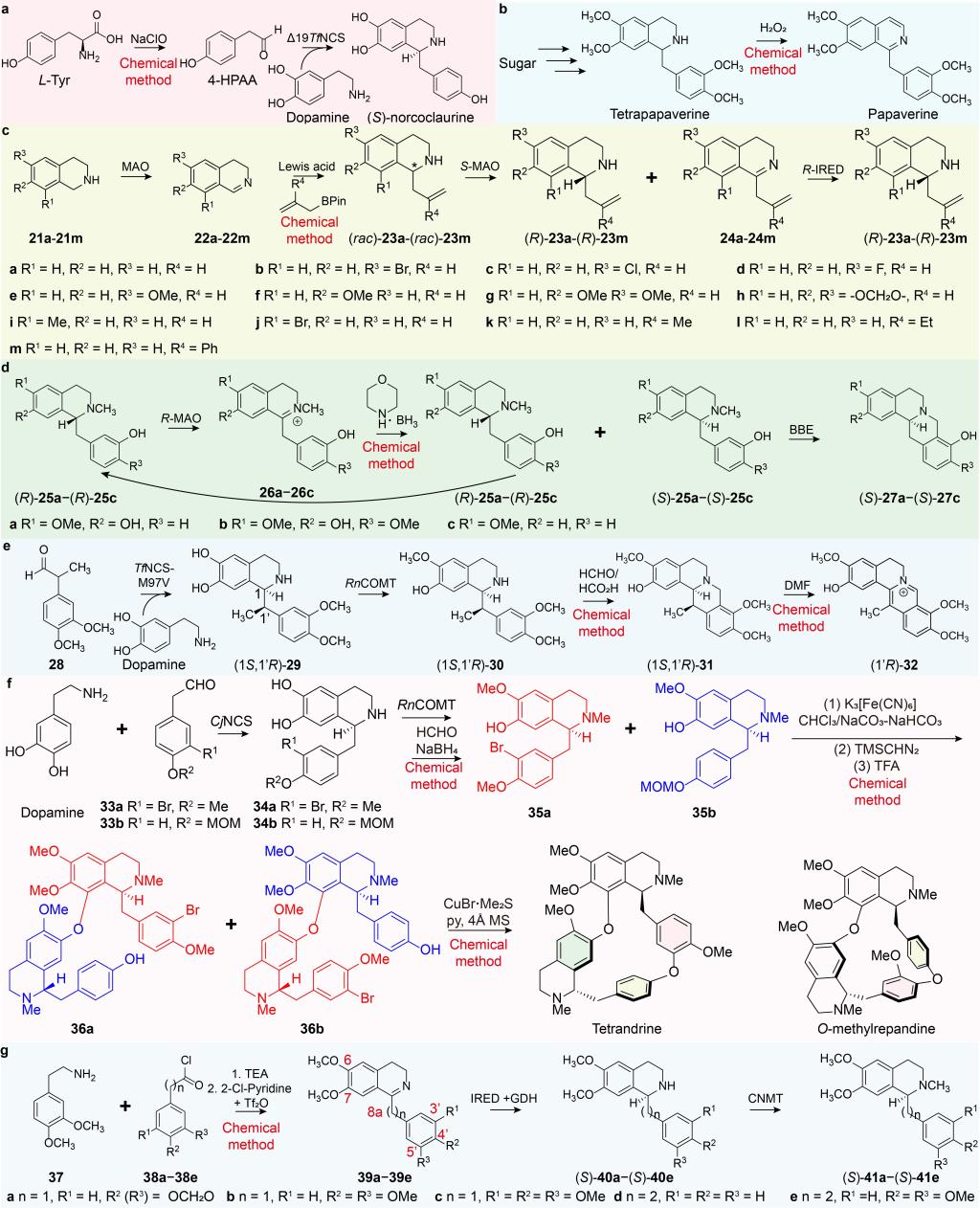
图3 合成THIAs的化学酶级联反应
本项目得到国家重点研发计划(2021YFC2100100)、国家自然科学基金(32270082和22108122)、江苏省自然科学基金(BK20202002)和中央高校基本科研业务费专项资金(JUSRP124020)项目资助。565net必赢客户端饶义剑教授和罗正山副研究员为共同通讯作者,原565net必赢客户端2019级博士研究生为论文第一作者。
近年来饶义剑教授团队围绕“天然产物的途径解析、仿生定向合成与应用”开展了系统性的研究,并取得了一系列原创性研究成果,部分成果已发表在Nature Communications (2023,2024,2025)、J Am Chem Soc(2024)、Angew (2022, 2023,2024)、ACS Catalysis (2020,2021,2022,2024)、Green Chemistry (2019, 2022)、Water Research (2022)、Journal of Hazardous Materials (2021, 2023)、Chemical Engineering Journal (2021)等本领域权威期刊。
