近期,我校565net必赢客户端夏小乐教授团队在微生物来源谷氨酰胺转氨酶(MTG)的改造与应用研究中取得新进展,研究结果“Analysis of structural, functional properties and interaction mechanism of soy protein gel induced by high-performance microbial transglutaminase”正式发表于Food Hydrocolloids(一区TOP期刊,IF=11.0) (https://doi.org/10.1016/j.foodhyd.2025.111170)。

谷氨酰胺转氨酶(TG酶)是一种能催化酰基转移反应的转移酶,可以通过催化蛋白质分子中 γ-羧酰胺基,实现蛋白质分子内和分子之间的交联。目前,微生物来源的TG酶(MTG)已经作为一种新型的食品添加剂,在世界范围的食品工业中广泛应用。它能通过凝胶化、乳化和增强水结合能力等作用方式,使形成的大豆分离蛋白(SPI)凝胶的质地和稳定性得到增强。但是,使用MTG诱导形成SPI凝胶目前主要存在两个问题。第一个问题在于MTG原产菌株产生的酶活力不高且热稳定性较差,容易在复杂的加工过程中失去活性。因此,获得高活性和热稳定性的MTG对扩大其应用范围具有重要意义。第二个值得注意的问题是,目前的研究主要集中在测定MTG交联形成SPI凝胶的各种功能性质上,而MTG与SPI两者之间的相互作用机制却鲜少有人进行深入探索。清楚地了解二者的相互作用机制可以帮助我们更好地提高产品质量,甚至还可以为酶交联蛋白技术开辟出新的应用领域从而推动食品工业的进步。
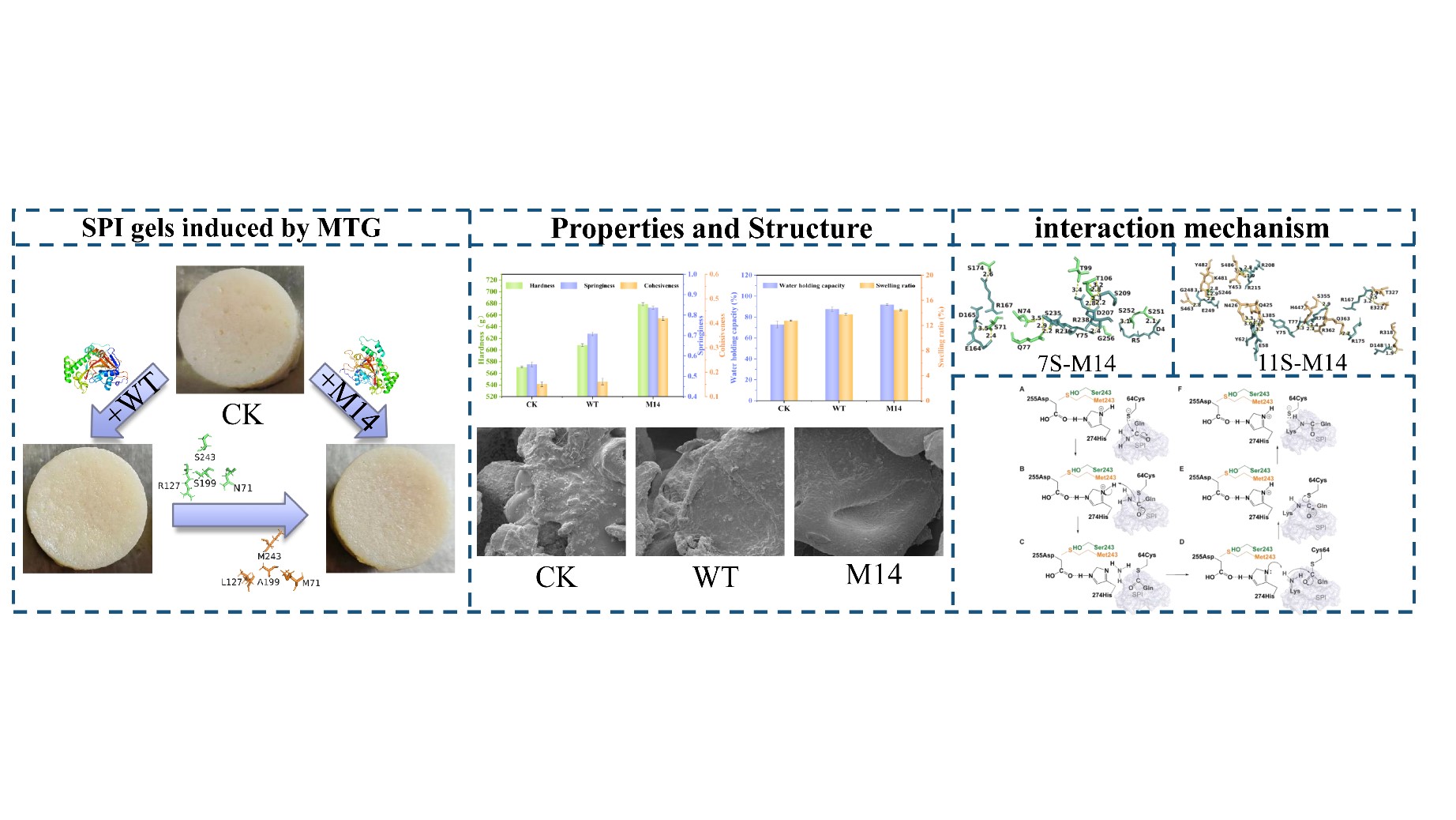
针对以上问题,我们开发了一种基于计算技术的空腔工程策略,以筛选出具有高催化活性和热稳定性的突变体。其中, N71M/S243M/S199A/R127L(M14)是比酶活得到显著提高的最优突变体,其比酶活 (354.40 U/mg)比野生型增加了14.45倍。同时,它的 Tm值增加了1.2℃,半衰期增长至62.6 min。结果表明,该突变体诱导形成SPI凝胶的各项理化性质(如质构特性、水合性质、流变性、热稳定性等)都有了明显提升。通过扫描电子显微镜(SEM)可以观察到,改性后的大豆分离蛋白凝胶有着更加致密且规则的网状结构。由分子动力学(MD)模拟可以看出,突变体M14的M71和M243残基使得所形成的复合物结合更加稳定。这些发现在拓宽SPI凝胶在食品的制造和加工应用方面起到了重要作用。
565net必赢客户端2022级硕士生邓宇和助理研究员高玲为共同第一作者,夏小乐教授为论文通讯作者。上述研究得到了国家重点研发计划(2023YFF1103703;2021YFC2104001)、中国博士后科学基金(2024M751150)以及中央高校基本科研业务费专项基金(JUSRP122037)等项目资助。
近年来,夏小乐教授在生物大分子元件改造及食品健康领域的应用取得了丰硕成果,相关研究发表在Nature Communications(2025)、Trends in Food Science & Technology(2024,2020)、Biotechnology Advances(2024)、Biosensors and Bioelectronics(2022)、Food Hydrocolloids(2024,2023)、Critical Reviews in Food Science and Nutrition(2022)、 Food Chemistry(2023)、Journal of Agricultural and Food Chemistry(2024,2023,2022)等本领域权威期刊。
